Forschung kann Leben retten. Vor allem Medikamente gegen seltene Krankheiten, sogenannte Orphan Drugs, sind ein Segen für die Betroffenen und oft deren einzige Hoffnung. Das Arzneimittelmarktneuordnungsgesetz (AMNOG) von 2011 strebt an, Preise für neue Arzneimittel an deren Nutzen zu orientieren. Der AMNOG-Report 2022 der DAK-Gesundheit zeigt jedoch, dass diese Grundidee zunehmend aus dem Fokus gerät. Die Folge ist eine Preisexplosion. Daher muss das AMNOG-Verfahren dringend auf den Prüfstand.

Das AMNOG sieht vor, dass auf Grundlage möglichst umfassender empirischer Daten zur Wirksamkeit ein Preis vereinbart wird, der für Pharma-Unternehmen einerseits und die Solidargemeinschaft andererseits akzeptabel ist. Orphan Drugs wurden jedoch aus der frühen Nutzenbewertung ausgenommen, sodass diese bereits durch ihre Zulassung einen Zusatznutzen bescheinigt bekommen.
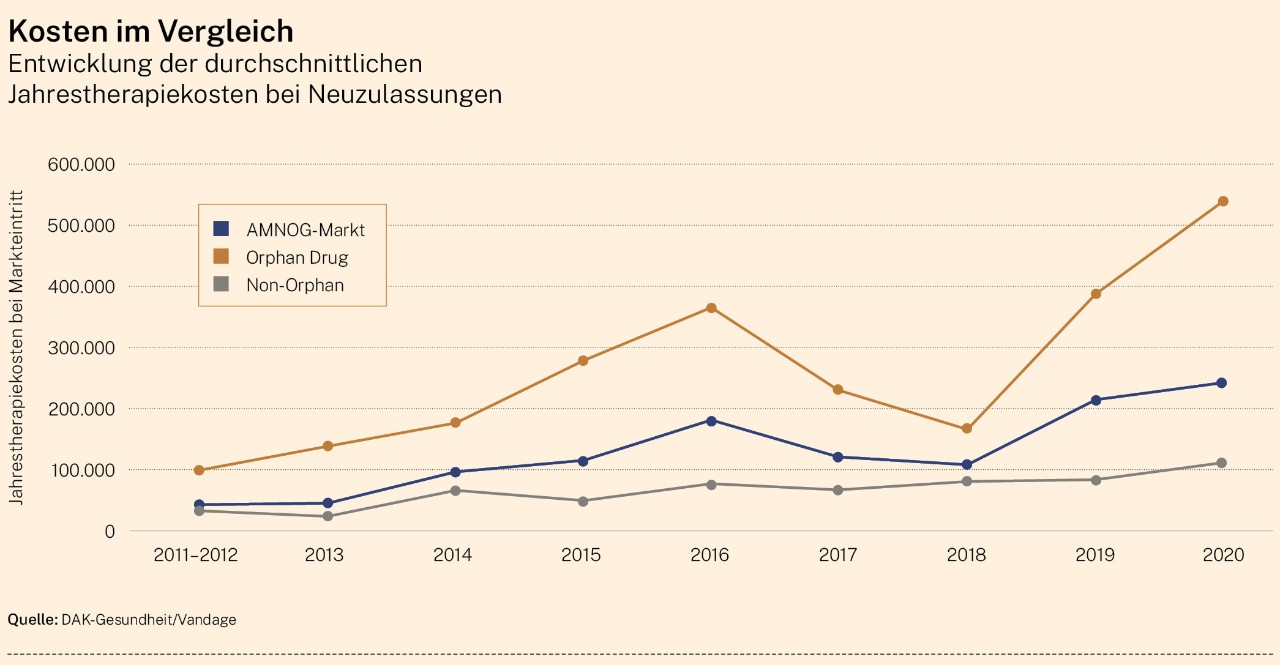
Dass die Daten nicht ausreichen, verdeutlicht der AMNOG-Report 2022. Er zeigt, dass bei Orphan Drugs nicht nur bei Markteintritt in der Regel zu wenige und qualitativ unzureichende Daten über den tatsächlichen Nutzen zur Verfügung stehen. Für knapp die Hälfte aller Orphan Drugs, nämlich 46 Prozent, konnte seit 2011 zudem nicht einmal ein Zusatznutzen festgestellt werden, sobald sie einer regulären Nutzenbewertung unterzogen wurden. Dies ist über den gesamten Zeitraum seit Bestehen des AMNOG zu beobachten und setzt sich weiter fort. Gleichzeitig steigen nicht nur die Jahrestherapiekosten gerade für diese Arzneimittel immer weiter an, auch ihr Anteil am Gesamtmarkt wird immer größer. Insgesamt waren 28 Prozent aller seit 2011 neu zugelassenen Arzneimittel Orphan Drugs, mit weiter steigender Tendenz. Davon entfiel mit 41 Prozent fast die Hälfte auf den Bereich der Onkologie.
Diese Preisentwicklung belastet das Solidarsystem zunehmend. Deshalb fordert DAK-Chef Andreas Storm, dass auch für Orphan Drugs spätestens ab Markteintritt verpflichtend valide Daten zum Zusatznutzen erhoben werden. Bis die Datengrundlage für eine Evaluation des Zusatznutzens ausreichend ist, könnte zukünftig ein Interimspreis zwischen Herstellern und der Solidargemeinschaft gelten. Dieser muss an klar definierte Kriterien geknüpft sein und gilt so lange, bis ausreichend Daten für eine Nutzenbewertung vorliegen. Ein auf Basis dieser Daten vereinbarter Preis löst dann den Interimspreis ab. Um den Anreiz für eine rasche Datengenerierung durch die Pharmaunternehmen zu setzen, sollte es eine Beschränkung einer nachträglichen Rückzahlung geben: Diese wäre dann nur für einen fest definierten Zeitraum möglich. So würde ein fairer Risikoausgleich zwischen Pharmaunternehmen und Krankenkassen bzw. privaten Versicherungen geschaffen.
Bereits im AMNOG-Report 2020 forderte der jetzige Gesundheitsminister Karl Lauterbach eine solche Interimspreis-Lösung und auch der Koalitionsvertrag der Ampel-Regierung sieht eine Reform des AMNOG vor. Die Politik steht also in der Pflicht, hier nachzusteuern. Nur so kann auch in Zukunft die Versorgung mit neuen Therapien und Arzneimitteln für alle gewährleistet werden, die diese dringend benötigen.













 Gesunde Lebenswelten – Ein Angebot der Ersatzkassen
Gesunde Lebenswelten – Ein Angebot der Ersatzkassen Landesbasisfallwerte 2025
Landesbasisfallwerte 2025 ICF – Internationale Klassifikation der Funktionsfähigkeit, Behinderung und Gesundheit
ICF – Internationale Klassifikation der Funktionsfähigkeit, Behinderung und Gesundheit Beitragsbemessungs- grenzen und Beitragssätze 2024
Beitragsbemessungs- grenzen und Beitragssätze 2024 Heilmittelversorgung – Verträge und Vergütungen
Heilmittelversorgung – Verträge und Vergütungen


